Traducción de Gabriel Onesko publicada en julio de 2023 | Texto original en portugués
Alerta Covid-19: texto original de agosto de 2020 puede contener información desactualizada!
Investigadores del Laboratorio de Microbiología Molecular de la Universidad Federal de Paraná (UFPR), Sector Litoral, compararon el desempeño de la prueba inmunológica de COVID-19 desarrollada por el equipo con el de la tradicional prueba Elisa [Enzyme-Linked Immunosorbent Assay], considerada el estándar de oro para los inmunoensayos.
La conclusión fue que el método de Paraná es más preciso y rápido. Además, el estudio revela que la nueva tecnología tiene potencial para ser utilizada en puntos de atención sanitaria y puede adaptarse para el diagnóstico de otras enfermedades. El coordinador del laboratorio, el profesor Luciano Fernandes Huergo, es el responsable de dirigir la investigación.
La prueba creada por los científicos de la UFPR es una adaptación de la tradicional prueba Elisa. La diferencia es que el proceso ya no se realiza en la superficie de una placa de plástico, sino en nanopartículas magnéticas recubiertas de antígenos virales. La técnica permite reducir el tiempo de reacción (interacción entre el antígeno y el anticuerpo) proporcionando un procedimiento más rápido.
Mientras la Elisa tradicional tarda unas tres horas en presentar el resultado, la nueva prueba solo necesita 12 minutos. Además de eso, con la ayuda de sistemas robóticos disponibles en el mercado, puede adaptarse para analizar hasta 96 muestras simultáneas, llevando los mismos 12 minutos para el resultado.
Cómo funciona la nueva prueba rápida
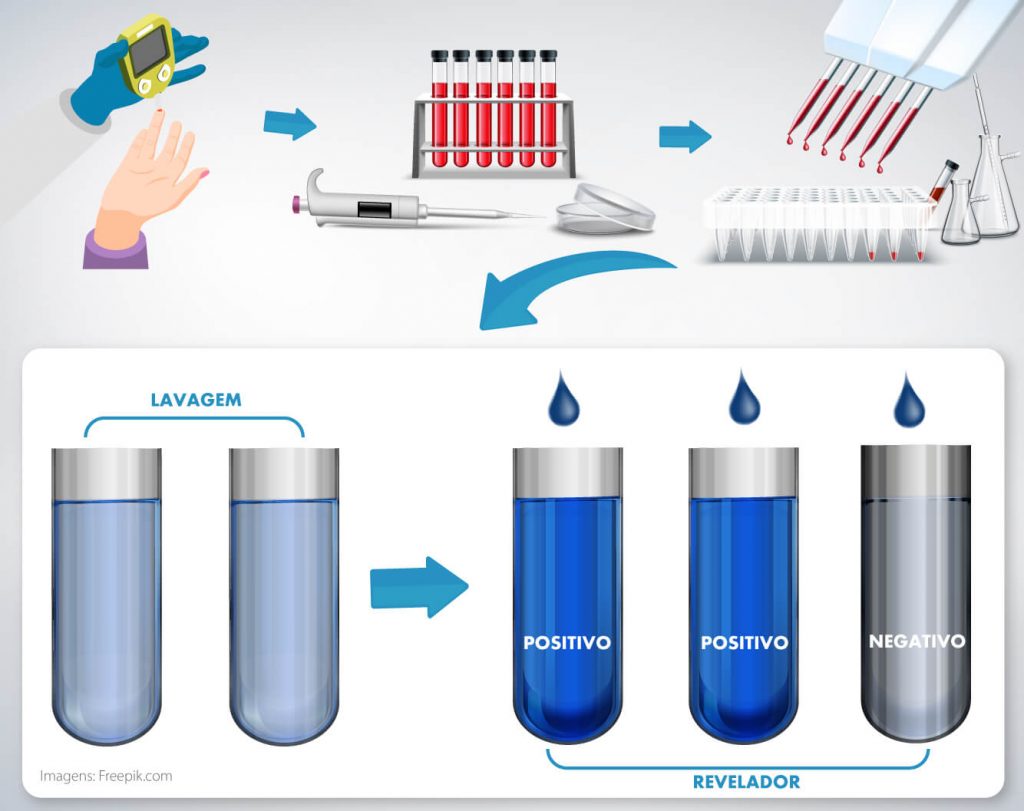
Para realizar la prueba, se necesita un volumen muy bajo de sangre, que se puede recoger con una lanceta como la que se utiliza para la prueba de la glucosa. Solo se necesitan dos microlitros de la fracción soluble, conocida como suero, y también es posible utilizar la sangre del paciente.
Se incuba esta muestra con los antígenos virales que se movilizan en la superficie de las nanopartículas magnéticas. Tras unos dos minutos en esta fase, se realizan etapas de lavado y luego se agrega un revelador, responsable por cambiar el color del material si hay una reacción positiva. Así, si el paciente ha desarrollado anticuerpos contra el coronavirus, la muestra presentará una mancha que indica el resultado positivo.
En general, los anticuerpos contra el nuevo coronavirus (Sars-CoV-2) alcanzan una estabilización entre 11 y 16 días después del inicio de los síntomas. Sin embargo, algunos pacientes producen anticuerpos detectables entre dos y cuatro días. Por lo tanto, estas pruebas inmunológicas pueden ser útiles como herramientas adicionales para identificar a los pacientes en la fase aguda de la COVID-19 o a aquellos que dieron falso negativo en la prueba PCR.
“La gran ventaja sobre la prueba rápida tradicional de inmunocromatografía es que el resultado de color en la prueba de la UFPR es directamente proporcional a la cantidad de anticuerpos. Es decir, el ensayo proporciona datos sobre la cantidad de anticuerpos y no solo sobre su presencia o ausencia, como ocurre con la prueba rápida tradicional”, revela Huergo.
Los científicos comparan la nueva prueba rápida a la Elisa
Para comprobar la eficacia de la nueva prueba, los investigadores recogieron muestras de pacientes del Complejo Hospitalario de Clínicas (CHC) de la UFPR a los que se les confirmó el COVID-19 por PCR. Las muestras negativas se obtuvieron del banco de donantes del hospital a partir de la sangre recogida de personas sanas en 2018.
El material recogido pasó tanto por la tradicional Elisa como por la prueba creada en la UFPR. Según Huergo, en la Elisa regular las pruebas de los pacientes positivos al COVID-19 mostraron una fuerte reacción con los antígenos, mientras que los negativos, una pequeña reacción cruzada. En la tecnología basada en nanopartículas magnéticas, los sueros positivos mostraron una fuerte reacción con los antígenos y los negativos no tuvieron reacción cruzada detectable.

«Nuestra prueba se comportó mejor que la Elisa clásica, especialmente en el caso de las muestras con títulos bajos de anticuerpos. La prueba clasificó correctamente 49 de las 50 muestras positivas de COVID-19 analizadas y demostró que no hubo falsos positivos en las más de 140 muestras negativas», afirma el profesor. Aunque se obtenga una mayor precisión con el uso de un lector de microplacas, los resultados positivos y negativos pueden observarse por inspección visual sin necesidad de instrumentación.
Después de una reciente revisión de diferentes técnicas serológicas para diagnosticar la enfermedad, los investigadores concluyeron que todos los métodos descritos tardaron mucho más en dar resultados que la tecnología que desarrollaron.
“En la literatura no existen registros de una prueba inmunológica rápida para COVID-19 que proporcione datos cuantitativos de manera tan rápida, con alta precisión y a bajo costo. Creemos que la técnica puede representar un nuevo hito en las pruebas inmunológicas y que pronto sustituirá a la tradicional Elisa, que se viene utilizando desde los años 70 cuando se describió por primera vez”, evalúa Huergo.
Entre las ventajas, más precisión (menos falsos positivos) y mayor rapidez
Para el equipo de científicos, la prueba que crearon tiene muchas ventajas sobre la prueba inmunológica estándar de oro que se usa en la actualidad. La primera de ellas está relacionada con la cantidad de material necesario para el análisis: una sola gota que contiene dos microlitros de suero. También es posible utilizar sangre sin tener que pasar por la fase de separación de la parte soluble.
Las reacciones se pueden interpretar mediante inspección visual, lo que facilita el análisis en los puntos de atención sanitaria, sin necesidad de llevarla al laboratorio o instrumentación específica. El tiempo total de reacción es 15 veces más corto que el de la prueba clásica, lo que da lugar a una prueba mucho más rápida que tarda 12 minutos en total y puede procesar cientos de muestras en pocas horas.
El antígeno, creado en el laboratorio del equipo, puede reproducirse a gran escala, sin necesidad de sofisticados instrumentos de laboratorio y a un costo muy bajo. Esto abarata el valor de la prueba, cuyos insumos de producción cuestan aproximadamente R$ 5,00.
«Creemos que el método barato, rápido y cuantitativo para detectar anticuerpos humanos contra el Sars-CoV-2 descrito en este estudio puede ayudar a detectar los casos de COVID-19 especialmente en países en desarrollo como Brasil. El ensayo requiere pasar por una instrumentación mínima en todas las etapas de producción y estará listo para ser evaluado con un mayor número de muestras, así como para la producción en masa”, defiende el investigador.
La tecnología, que está disponible para asociaciones de Investigación, Desarrollo e Innovación (I+D+I) y para transferencia de tecnología a través de la Agencia de Innovación de la UFPR, ya tiene el registro de la patente. Los científicos están buscando socios para realizar la producción a gran escala.